泰博医疗-专业的儿科医疗连锁机构
作者: 发布时间:2017-04-18 转至微博:
|
医药网4月15日讯 4月13日,国家药监总局药品审评中心发布《拟纳入优先审评程序药品注册申请的公示(第十五批)》 ,将9个拟优先审评的药品注册申请及其申请人予以公示,公示期5日。
公示期间如有异议,请在审评中心网站“信息公开→优先审评公示→拟优先审评品种公示”栏目下提出异议。
从申请事项来看,此次公示的名单中,有2个新药临床试验、3个新药上市、4个仿制药上市,涉及勃林格殷格翰、北京凯因科技、葛兰素史克、百傲万里、成都蓉生药业、恒瑞、石药集团欧意药业7家。
值得关注的是,拟纳入优先审评的4个仿制药上市申请有恒瑞医药的苯磺顺阿曲库铵注射液,以及石药集团欧意药业的3个盐酸二甲双胍片,理由均是同一生产线生产,已在美国上市,申请国内上市的仿制药。
据了解,2017年2月7日,恒瑞医药公告,该公司产品苯磺顺阿曲库铵注射液获得美国FDA批准文号,具备了在美销售该产品的资格。石药集团欧意药业的盐酸二甲双胍(缓释片)、盐酸二甲双胍(片剂)分别于2008年4月17日、2016年7月11日在美国获批上市。
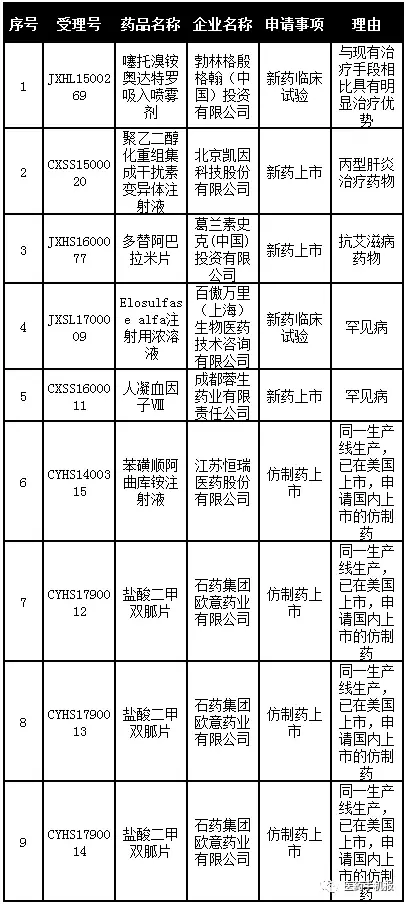
第十五批拟纳入优先审评程序药品注册申请公示名单如下:
关键词:
|